|
Vergleich
der Siedepunkte und der WL von
Alkoholen, Aldehyden, Ketonen und Ethern gleicher C-Zahl |
|||||
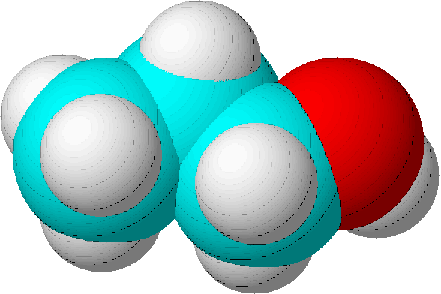
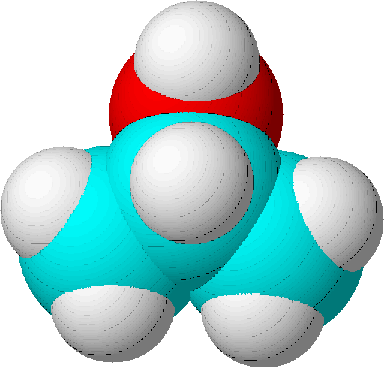
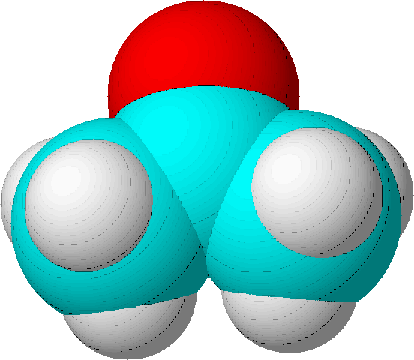
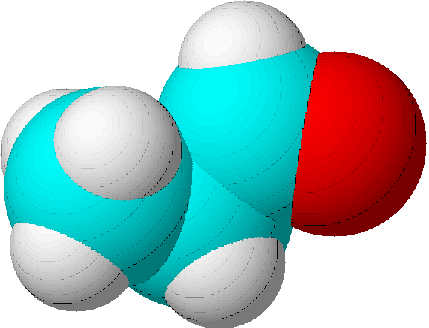
| Namen | 1-Propanol | 2-Propanol | Propanon | Propanal | Ethyl-methyl-ether |
 |
 |
 |
 |
 |
|
| Summenformel | C3H8O | C3H8O | C3H6O | C3H6O | C3H8O |
| Molare Masse [g/mol] | 60,1 | 60,1 | 58,1 | 58,1 | 60,1 |
| Siedepunkt [°C] | 97,2 | 82,3 | 56,1 | 47,9 | 7,4 |
| Begründung | WBB, bei 1-Propanol am Ende, wirkt sich deswegen voll aus, bei 2-Propanol in der Mitte: die hydrophile Gruppe wird von 2 hydrophoben Gruppen flankiert | keine WBB untereinander, da NOF-Regel nicht erfüllt. DDB stärker im Keton als im Aldehyd, weil sie sich auf zwei gleich große Gruppen auswirkt. VdWK: sehr gering! | Relativ schwache DDB und VdWK, geringe Polarität | ||
| Wasserlöslichkeit | unendlich | unendlich | unendlich | 16 g/100 g Wasser | 5 g/100 g Wasser |
| Begründung | alle drei Moleküle bilden mit Wasser WBB, die hydrophoben Reste sind zu klein, um massiv zu stören; Alkohole erlauben WBB von beiden Komponenten der OH-Gruppe aus (H-und O-Atom) | WBB eingeschränkt, da nur das O-Atom WBB ermöglicht und der KW-Rest massiv hydrophob ist | Nur das O-Atom ermöglicht schwache WBB, da die KW-Reste massiv stören | ||
|
Aussagen zur Aufgabe I: Beurteile die
Aussagequalität! ■ „Kräfte können optimal wirken“ ■ „Stoffe mit fast gleicher Struktur haben auch fast gleiche Eigenschaften“ ■ „Die Dipol-Dipol- bzw. WBB sorgt bei den Alkoholen, den Aldehyden bzw. Ketonen, Ethern und Carbonsäuren für die hohen Siedetemperaturen, da die Bindungskräfte das Verlassen der flüssigen Phase erschweren.“ ■ „Das Aldehyd hat zwar auch eine WBB, jedoch ist sie nicht so ausgeprägt, da das Sauerstoffatom doppelt an den Kohlenstoff gebunden ist. ■ „Das selbe gilt auch für den Ether.“ ■ |
|||||
| update am: 02.02.21 zurück zur Hauptseite | |||||