|
Lösungen:
a)
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
b)
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
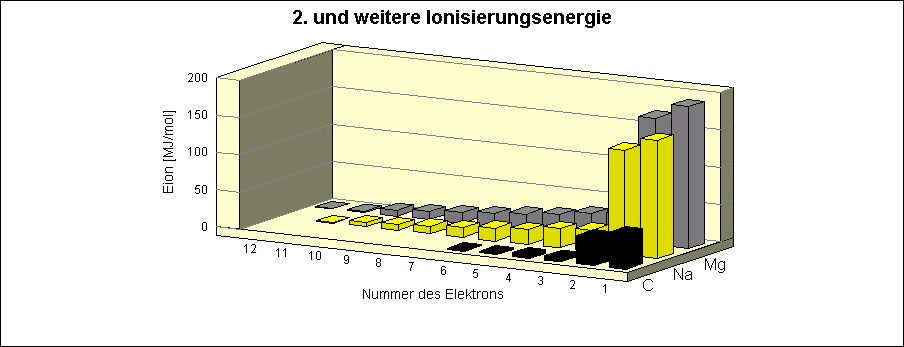
Bei allen drei Elementen gibt es eine
Gruppe von zwei Elektronen mit der höchsten Ionisierungsenergie. Danach
folgt -
soweit vorhanden, eine 2. Gruppe mit maximal 8 Elektronen, die sich von
der ersten und einer ev. vorhandenen dritten
Gruppe unterscheiden. Als letztes folgt die Gruppe mit den niedrigsten
Ionisierungsenergien, bei Magnesium mit 2 Elektronen,
bei Natrium mit einem Elektron. Die höchste Ionisierungsenergie erhalten
immer die Elektronen mit der Nummer 1 und 2.
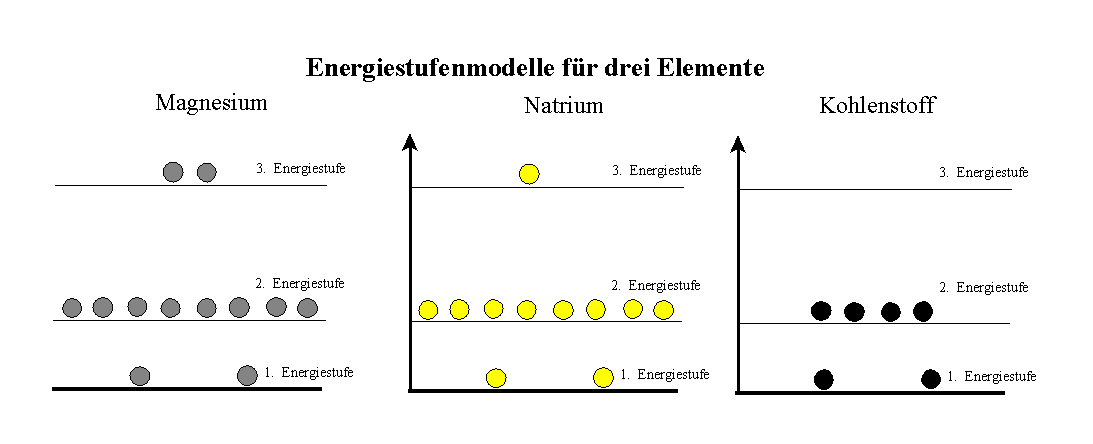
Das Verteilungsmuster gleicht den Mustern aus den Graphiken anderer Elemente mit mehr als 10 Elektronen, z.B. Neon, Aluminium oder Schwefel, siehe auch Ionisierungsenergie (II) c) Energiestufenmodell für Magnesium, Natrium und Kohlenstoff
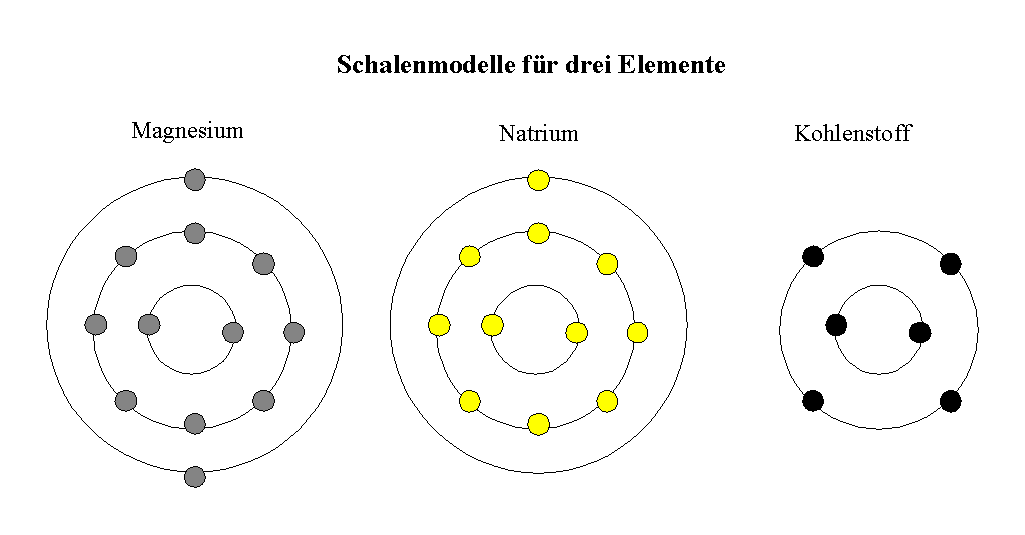
d) Schalenmodell für Magnesium, Natrium und Kohlenstoff
|
| update am: 02.02.21 zurück zur Hauptseite |